首先我們應該明確一點���,疫苗作為人類醫(yī)學最偉大的發(fā)明之一����,每年都能拯救數(shù)百萬的生命����。縱然由于目前個別批次疫苗存在問題,我們也不能否認疫苗本身的正面作用����。
而對于制藥企業(yè)本身而言�,生產(chǎn)記錄這一個小小的方面對于藥品質(zhì)量究竟有多重要則不言而喻���。

 生產(chǎn)記錄是產(chǎn)品的“身份證”
生產(chǎn)記錄是產(chǎn)品的“身份證”
一般來說�����,一份生產(chǎn)記錄主要包括:供應部門的原輔料進貨記錄���;倉儲原輔料以及產(chǎn)品的進����、出貨記錄�����;財務部門的相應原輔料購買憑證和記錄����;質(zhì)檢部門相應的原輔料以及產(chǎn)品的取樣記錄����、檢驗記錄、檢驗報告單等;生產(chǎn)部門的領用記錄����、批生產(chǎn)記錄;銷售部門產(chǎn)品調(diào)出記錄等���。
其內(nèi)容包括產(chǎn)品名稱、生產(chǎn)批號、生產(chǎn)日期�����、操作者與復核者的簽名�����、有關操作與設備�����、相關生產(chǎn)階段的產(chǎn)品數(shù)量����、物料平衡的計算��、生產(chǎn)過程的控制記錄及特殊問題記錄�����。一旦產(chǎn)品出現(xiàn)問題,這些記錄便可以查找企業(yè)生產(chǎn)存在的問題,掌握產(chǎn)品的去向���,可是如此關鍵的生產(chǎn)記錄卻被人動了手腳,這種造假不僅暴露出企業(yè)管理不善,而且存在著巨大危害。
所以關于數(shù)據(jù)可靠性的問題不僅是此次事件的癥結所在,更一直都是各類現(xiàn)場檢查���、跟蹤檢查、飛行檢查等各類檢查的重中之重。
 什么是數(shù)據(jù)可靠性�?
什么是數(shù)據(jù)可靠性�?
數(shù)據(jù)可靠性指在數(shù)據(jù)生命周期內(nèi)����,數(shù)據(jù)完整��、一致、準確的程度�����。應當以安全的方式收集和維護數(shù)據(jù)����,從而保證數(shù)據(jù)歸屬至人、清晰可溯�、同步記錄�����、原始一致、準確真實(國際上�,常用縮略詞“ALCOA”或“ALCOA+”概括)����。

在《2017年度藥品檢查報告》中國家藥品監(jiān)督管理局共計完成了751項各類檢查����。
其中國家藥品監(jiān)督管理局發(fā)現(xiàn)的可靠性相關的問題主要包括:修改系統(tǒng)時間后檢測、關鍵數(shù)據(jù)無法溯源���,原始記錄、原始圖譜�、原始數(shù)據(jù)及計算過程缺失�����,檢驗原始記錄內(nèi)容不一致,惡意修改積分參數(shù)����,套用圖譜,生產(chǎn)和檢驗記錄管理混亂�����,提前填寫記錄�,未對分析儀器的計算機系統(tǒng)進行權限管理和有效控制等。
國家藥品監(jiān)督管理局對藥品生產(chǎn)數(shù)據(jù)的可靠性進行審計的重點是:
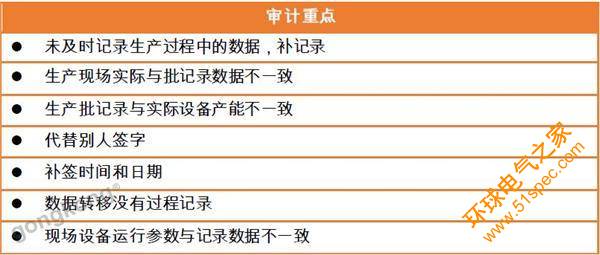
相關的檢查清單:

由此可見確保整個制藥生產(chǎn)過程的數(shù)據(jù)可靠性��,這已成為全球藥企合規(guī)性的基礎��,并成為監(jiān)管部門重點核查的領域���。
 看到這里您肯定會問
看到這里您肯定會問
那么梅特勒-托利多又能做些什么����?
梅特勒-托利多基于現(xiàn)有相關數(shù)據(jù)完整性法規(guī)的要求���,幫助制藥廠家針對制藥的整個生產(chǎn)流程:
從實驗室原料��、成品的稱量及分析��;原料���、輔料配料混合攪拌��;工藝參數(shù)控制;罐裝��、壓片或制粒�;到藥品包裝與物流提供不同層次的解決方案,
使用部分或全部無紙化系統(tǒng)解決方案來管控生產(chǎn)流程��,確保制藥企業(yè)及時���、準確的記錄��,實現(xiàn)相關數(shù)據(jù)的追溯和安全存儲。

【原料�����、成品實驗室檢驗環(huán)節(jié)】
對于實驗室常見的中小型儀器�,諸如密度、折光���、電導率、pH計、滴定��、水分���、天平等梅特勒-托利多產(chǎn)品系列����,可以利用LabX軟件整合在同一個操作平臺上進行統(tǒng)一管理。

LabX提供多樣化的用戶管理、集中化的數(shù)據(jù)管理和統(tǒng)一化的SOP方法管理。用戶不僅可以在電腦屏幕控制儀器進行分析��,而且可以在儀器觸摸屏調(diào)用相關方法�,按照屏幕提示步驟操作即可,無需人工計算,無需紙質(zhì)版SOP�,實驗數(shù)據(jù)自動上傳到安全的數(shù)據(jù)庫中�,消除計算和轉錄的錯誤���,有助于滿足ALCOA原則規(guī)范����,實現(xiàn)檢驗數(shù)據(jù)可靠性。
【在工藝控制環(huán)節(jié)】
梅特勒-托利多過程分析部門的智能傳感器管理(ISM)技術���,幫助優(yōu)化在線傳感器的管理和使用;同時�,配套的軟件iSense�,可有效采集���、分析和管理電極的校準信息并保持連貫記錄���。iSense CFR在技術上符合21CFR第11部分和EudraLex第4卷附錄11的要求�����,幫助企業(yè)在確保生產(chǎn)速度的同時最大限度提升產(chǎn)品質(zhì)量,保障客戶的利益��,最大限度的確保制藥企業(yè)的數(shù)據(jù)完整性與可靠性��。
同時�����,可提供完整的電子文件記錄并進行用戶管理。將諸如校準或維護等與傳感器相關的所有活動進行存儲�,并通過電子方式或打印方式進行文件記錄��;另外,用戶管理與電子日志簿可控制與跟蹤各項活動��,以確保在傳感器資產(chǎn)的整個使用壽命期內(nèi)對其進行完整文件記錄�。憑借可輕松訪問的,關于每一臺傳感器的完整與可靠文件��,可以很容易地滿足法規(guī)要求�。
【在制藥的生產(chǎn)環(huán)節(jié)】
稱重是藥品生產(chǎn)中的重要過程,我們從標簽打印、數(shù)據(jù)采集、配料稱量和質(zhì)量管理等方面提升數(shù)據(jù)的可靠性�,確保符合GMP要求����。

我們的ICS689標簽打印解決方案,幫助制藥企業(yè)打印完整的原始數(shù)據(jù)及元數(shù)據(jù),方便物料核對和復核,配合Collect+數(shù)據(jù)采集軟件����,實現(xiàn)自動化數(shù)據(jù)傳輸�����,避免轉錄錯誤��。
在配料稱量環(huán)節(jié)�����,我們的FormWeigh.Net配方稱量系統(tǒng)是一套合規(guī)的聯(lián)網(wǎng)系統(tǒng),實時監(jiān)控�����、控制�、追蹤并驗證配制工藝的各個方面,系統(tǒng)具備鎖定時間戳����,權限分級��,審計追蹤等功能,確??煽客暾挠涗?���,避免人為修改�����,全流程可追溯���。
安全的藥品生產(chǎn)離不開全面的質(zhì)量控制�����,我們的FreeWeigh.Net質(zhì)量控制解決方案通過系統(tǒng)地采集質(zhì)量數(shù)據(jù)���、統(tǒng)計分析�����、編制文檔和監(jiān)控生產(chǎn)過程��,幫助企業(yè)更好的控制藥品的質(zhì)量。
【在制藥生產(chǎn)成品包裝前后環(huán)節(jié)】
梅特勒-托利多的Tablex金屬檢測機提供符合FDA 21 CFR part 11的嚴格規(guī)定的電子簽名及生產(chǎn)日志,多級密碼權限,防止越級操作���,可確保所有操作追溯到人,從而支持完全符合標準要求,使得生產(chǎn)企業(yè)可以始終全面掌控藥品的生產(chǎn)過程�。

對于制藥企業(yè)來說����,符合質(zhì)量標準的藥品=合格的操作人員+符合要求的設備+良好的流程
如何符合法規(guī)�,控制風險,確保質(zhì)量�,把人為差錯降到最低�����,杜絕造假,防患于未然���,是贏得市場和用戶信任的關鍵。
梅特勒-托利多希望通過我們的解決方案��,幫助制藥企業(yè)完善GMP流程�����,重鑄市場信心���。